18 marzo 2026
Tempo di lettura [minuti]: 22
Diagnostica Distribuita
Diagnostica decentralizzata: efficienza operativa e clinica
Come la diagnostica molecolare point-of-care – grazie a PCR multiplex stabilizzate a temperatura ambiente, dispositivi portatili come bCUBE™ e gestione cloud via bAPP™ – migliora concretamente tempi di risposta clinici e processi operativi in sanità.
Abstract
Obiettivo
Dimostrare in modo misurabile come la diagnostica molecolare decentralizzata possa migliorare l’efficienza clinica e quella operativa nei percorsi assistenziali.[15]
Tecnologie chiave
PCR multiplex stabilizzate a temperatura ambiente.[1] Strumenti portatili di real-time PCR e gestione software cloud dei risultati.[2]
Risultati attesi
Tempi di risposta diagnostica ridotti da ore o giorni a finestre compatibili con la decisione clinica immediata, con alleggerimento del laboratorio centrale e maggiore tempestività degli interventi.[4]
Impatto
In contesti ospedalieri e territoriali, la letteratura documenta riduzioni marcate del TAT.[5] La maggiore tempestività può riflettersi su appropriatezza terapeutica, isolamento e organizzazione dei flussi.[6]
- Snapshot
- Introduzione
- 1. Riduzione dei tempi di risposta in PS, RSA e ambulatori
- 2. Meno sovraccarico logistico e centralizzato, più continuità operativa
- 3. Formazione semplificata, controllo di qualità automatizzato e operatività diffusa
- 4. Outcome clinici migliorati grazie a diagnosi tempestive
- 5. KPI e indicatori chiave: TAT, costo per test, produttività per FTE
- 6. Modelli regionali e ibridi: dall’hub & spoke al network diffuso
- 7. Conclusioni
Snapshot
PCR multiplex ambient-stabile
Tecnologie PCR in grado di rilevare simultaneamente più patogeni in un unico test, con reagenti formulati per restare stabili a temperatura ambiente. Eliminano la necessità della catena del freddo, facilitando logistica e stoccaggio anche fuori dal laboratorio.[1]
bCUBE™
Termociclatore portatile miniaturizzato per real-time PCR sviluppato da Helyx Industries S.p.A. – Divisione Hyris, parte della piattaforma Hyris System™.[2]
bAPP™
Piattaforma software cloud per la gestione e l’analisi dei risultati del sistema Hyris System™.[2]
Turnaround Time (TAT)
Indica il tempo di risposta di un test diagnostico, dall’esecuzione del prelievo al referto disponibile. Un TAT ridotto è cruciale per decisioni cliniche tempestive, specie in situazioni acute.[4]
Hub & Spoke
Modello organizzativo “a mozzo e raggi” in cui un laboratorio centrale (hub) supporta una rete di punti di test periferici (spoke). I test più urgenti possono essere eseguiti negli spoke, mentre l’hub centralizza analisi specialistiche, conferme o elaborazioni di seconda linea, garantendo standardizzazione e qualità.[12]
Introduzione
La capacità di diagnosticare rapidamente una patologia è fondamentale non solo per trattare tempestivamente i pazienti, ma anche per migliorare la sorveglianza epidemiologica e il controllo delle infezioni.[3] Durante la pandemia di COVID-19, i limiti di un approccio accentrato sono emersi con forza: affidarsi esclusivamente a laboratori centralizzati ha comportato ritardi nei referti, con impatti negativi sul flusso dei pazienti e sulla gestione dell’isolamento.[5] In generale, i tradizionali laboratori core offrono elevati volumi e standardizzazione, ma soffrono della distanza dal punto di cura: il tempo speso a trasportare campioni e attendere batch di analisi può erodere il vantaggio di velocità intrinseco di tecniche come la PCR.[4] Da questa constatazione nasce la spinta verso la diagnostica decentralizzata, il cui scopo è portare il test “al letto del paziente” anziché il paziente al test.[4]
Le soluzioni di decentralizzazione molecolare oggi disponibili mirano a coniugare l’accuratezza della diagnostica di laboratorio con la rapidità e l’accessibilità dei test rapidi. Nel perimetro di Helyx Industries S.p.A., la Divisione Hyris sviluppa un ecosistema di qPCR distribuita basato su bCUBE™ e bAPP™.[2] Nelle applicazioni validate del sistema Hyris pubblicate in letteratura, il risultato è stato ottenuto in meno di due ore senza la necessità di un laboratorio pienamente attrezzato.[13] In altri termini, la diagnostica molecolare può essere resa più distribuita, connessa e vicina al punto di cura, mantenendo una logica di gestione centralizzata dei dati e dei workflow.[2]
In questo articolo analizziamo come tale approccio decentralizzato migliori l’efficienza clinica ed operativa in modo tangibile. Presenteremo casi d’uso e indicatori chiave (TAT, costi, produttività) confrontando il modello tradizionale con quello distribuito. In particolare, approfondiremo: (1) la riduzione dei tempi di refertazione in pronto soccorso, RSA e strutture periferiche; (2) l’alleggerimento del carico dei laboratori centralizzati e della logistica dei campioni; (3) gli impatti su formazione del personale, controllo di qualità e continuità operativa; (4) i benefici clinici in termini di outcome grazie a diagnosi più tempestive; (5) alcuni KPI misurabili; (6) i modelli organizzativi regionali ibridi, con un riquadro comparativo “tradizionale vs distribuito”. Il tone of voice rimane prevalentemente tecnico (70%) per supportare i direttori di laboratorio e sanitari con dati e letteratura, ma con uno sguardo strategico (30%) utile a stakeholder regionali, OEM e investitori.
Prima di entrare nel dettaglio, vale la pena sottolineare come la diagnostica decentralizzata non sia più un concetto futuristico. Il mapping ECDC del 2022 documenta l’uso dei dispositivi POCT per malattie infettive in diversi Paesi europei e ne evidenzia il potenziale per sorveglianza, prevenzione e controllo.[3] Alla luce di queste premesse, passiamo ad esaminare i benefici operativi e clinici ottenuti portando il laboratorio più vicino al paziente.
1. Riduzione dei tempi di risposta in PS, RSA e ambulatori
Il Turnaround Time (TAT) è forse il parametro più importante per valutare l’efficienza clinica di un percorso diagnostico. Nei flussi tradizionali centralizzati, i campioni prelevati in pronto soccorso o in reparto vengono inviati al laboratorio, processati spesso in batch, e il referto arriva dopo molte ore o addirittura giorni. Questo ritardo può essere critico in situazioni acute: pazienti con sintomi respiratori o febbre devono attendere in isolamento o essere trattati empiricamente, con rischi di contagio e uso inappropriato di antibiotici o antivirali.[6] I test molecolari point-of-care, al contrario, possono ridurre drasticamente i TAT, portandoli in molti casi entro circa due ore e rendendo possibile una decisione clinica nella stessa finestra assistenziale.[4]
Uno studio emblematico in ambito COVID-19 (COV-19POC) ha mostrato che l’introduzione di test molecolari rapidi point-of-care in ospedale ha ridotto il tempo medio di refertazione da 21,3 ore a 1,7 ore, con una riduzione superiore al 90%.[5] Questo si è tradotto in benefici tangibili: meno pazienti trattenuti inutilmente in reparti di isolamento, più rapida allocazione nei reparti appropriati e una riduzione della durata della degenza per i negativi.[5] Anche in ambito non pandemico, Drancourt et al. riportano che i laboratori point-of-care possono fornire risultati entro due ore, rispetto a tempi di uno o due giorni per laboratori centralizzati, migliorando la gestione clinica e il controllo delle infezioni.[4]
In pronto soccorso, un TAT ridotto significa poter distinguere più rapidamente tra infezioni batteriche e virali, identificare patogeni specifici e iniziare terapie mirate prima che il paziente venga ricoverato o dimesso. La review sistematica di Mojebi et al. (2024) ha evidenziato che i test molecolari rapidi per virus respiratori in PS sono associati a riduzione dell’uso di antibiotici, minori tempi di isolamento e, in alcuni studi, riduzione delle ospedalizzazioni.[6]
Nelle RSA e nelle strutture long-term care, la rapidità diagnostica è cruciale per contenere focolai. I residenti sono spesso fragili e un’infezione respiratoria può diffondersi rapidamente con conseguenze cliniche rilevanti. In uno studio prospettico su contesti congregati, l’implementazione di un testing molecolare POC per virus respiratori ha consentito turn-around time più rapidi e una dichiarazione dell’outbreak più tempestiva.[7] Ciò rende possibili interventi di contenimento immediati – isolamento, screening dei contatti, profilassi quando indicata – riducendo l’impatto clinico e sociale.[7]
Anche negli ambulatori territoriali e nelle cliniche periferiche, la riduzione dei tempi di risposta migliora la qualità del servizio e la gestione del paziente. Un esempio rilevante viene dai programmi pubblici di early infant diagnosis dell’HIV in Africa: con il point-of-care, la diagnosi nello stesso giorno e l’avvio più rapido della terapia antiretrovirale sono risultati concretamente raggiungibili.[8] Il principio è più ampio: quando il risultato arriva nello stesso episodio assistenziale, la probabilità che la diagnosi si traduca subito in una decisione clinica utile aumenta in modo sostanziale.[15]
2. Meno sovraccarico logistico e centralizzato, più continuità operativa
Oltre ai tempi clinici, la diagnostica decentralizzata impatta profondamente l’efficienza operativa dei sistemi sanitari. I laboratori centralizzati devono gestire volumi elevati, picchi di richieste e una logistica complessa di campioni provenienti da sedi diverse. Ogni campione richiede trasporto, tracciamento, registrazione e spesso un processo batch per ottimizzare l’uso delle macchine. Questo crea colli di bottiglia logistici e amministrativi.[4]
Con un modello decentralizzato, parte del carico viene spostata direttamente nei punti di cura. I test eseguiti in PS o in RSA non devono essere trasportati, riducendo tempi e costi logistici. Inoltre, il laboratorio centrale può concentrarsi su analisi ad alta complessità, conferme e test specialistici, migliorando la qualità e la produttività complessiva.[4]
Un altro aspetto operativo chiave è la robustezza della filiera diagnostica in condizioni ambientali non ideali. In scenari tradizionali, reagenti e campioni devono spesso essere mantenuti refrigerati durante il trasporto per non degradare. La stabilizzazione e liofilizzazione dei reagenti PCR consente invece di ridurre la dipendenza dalla cold chain e di semplificare trasporto, stoccaggio e disponibilità dei kit fuori dal laboratorio centralizzato.[1] In uno studio su un master mix multiplex liofilizzato ready-to-use, la formulazione è risultata stabile senza perdita di performance analitica anche dopo esposizione a variazioni termiche di trasporto.[1] Per una piattaforma distribuita questo significa minore vulnerabilità logistica e maggiore continuità operativa nei punti periferici.[1]
La continuità operativa h24 è un ulteriore beneficio. I laboratori centralizzati spesso hanno orari limitati o richiedono turni notturni costosi per garantire servizio continuo. I dispositivi POC, invece, possono essere integrati in modelli operativi estesi, permettendo diagnosi più rapide anche di notte o nei weekend.[4]
3. Formazione semplificata, controllo di qualità automatizzato e operatività diffusa
Un’obiezione comune alla diagnostica decentralizzata è la necessità di personale specializzato. Tradizionalmente, la PCR richiede competenze tecniche, preparazione del campione e interpretazione dei risultati. Tuttavia, l’evoluzione tecnologica ha ridotto questi requisiti grazie a sistemi portatili e workflow integrati, pensati per coniugare rapidità, semplicità e robustezza operativa.[9] Questo consente di estendere l’operatività a personale non specialista, purché adeguatamente formato e inserito in procedure di qualità robuste.[10]
Helyx Industries declina questo approccio in una piattaforma integrata basata su bCUBE™ e bAPP™.[2] Nelle validazioni pubblicate sul sistema Hyris per SARS-CoV-2, la refertazione è risultata più rapida dei metodi di riferimento e compatibile con un impiego fuori dal laboratorio pienamente attrezzato.[13]
Sul fronte del controllo di qualità, la decentralizzazione molecolare moderna si regge su protocolli standardizzati, controlli interni e connettività con il laboratorio centrale.[4] Nei modelli decentrati con task shifting, la qualità del test può rimanere comparabile anche quando parte dell’operatività è affidata a personale non laboratorista, se il sistema è supportato da formazione e governance adeguate.[10]
In sistemi validati, le performance analitiche dei test molecolari POC possono risultare comparabili ai metodi di riferimento, con il vantaggio di un TAT significativamente più breve.[13] Il risultato è un’operatività più ampia: più sedi e più operatori coinvolti, ma sotto un unico ombrello di qualità coordinato centralmente.
4. Outcome clinici migliorati grazie a diagnosi tempestive
L’efficienza clinica non si misura solo in minuti risparmiati, ma in outcome migliorati. In microbiologia clinica, l’accesso a una diagnosi rapida e azionabile può influenzare le decisioni di cura in misura ben superiore al costo del test stesso.[15] Nel caso dei pazienti con sintomi respiratori, la review di Mojebi et al. (2024) ha evidenziato che i test molecolari rapidi possono ridurre l’uso improprio di antibiotici e migliorare la gestione clinica, soprattutto quando integrati in percorsi di stewardship.[6]
Nel caso di infezioni gravi come sepsi o meningite, ogni ora conta: ritardi diagnostici possono portare a terapia empirica non ottimale o a ritardi nell’inizio della terapia mirata, con possibile peggioramento degli esiti.[15] Anche se questo articolo usa le infezioni respiratorie come caso emblematico, la logica è trasversale: ridurre il TAT significa anticipare decisioni cliniche critiche.[15]
In ambito RSA e long-term care, la diagnosi rapida permette di isolare tempestivamente i positivi e prevenire focolai. Questo riduce non solo la mortalità potenziale, ma anche l’impatto sociale e organizzativo associato alla gestione di outbreak in popolazioni fragili.[7]
5. KPI e indicatori chiave: TAT, costo per test, produttività per FTE
Per valutare concretamente l’efficacia della diagnostica decentralizzata, è utile considerare alcuni KPI misurabili.
TAT medio: come già visto, i test POC molecolari possono ridurre il TAT da oltre 20 ore a meno di 2 ore in contesti ospedalieri.[5] In molti casi, la riduzione può superare il 90%, trasformando decisioni cliniche che richiedevano un giorno in decisioni entro la stessa visita o lo stesso accesso ospedaliero.[5]
Costo per test: valutare il costo “pieno” di un test diagnostico richiede di includere non solo reagenti e personale, ma anche logistica, tempi di degenza, isolamento, appropriatezza terapeutica e velocità di refertazione. In quest’ottica, la letteratura di modellizzazione su alcune applicazioni molecolari mostra che il POC può risultare costo-efficace e, in specifici scenari, anche costo-saving rispetto al modello centralizzato.[11] Il punto decisivo è che il costo unitario del reagente non esaurisce il costo reale del percorso diagnostico.[15]
Produttività per FTE (Full-Time Equivalent): la decentralizzazione può aumentare la capacità complessiva del sistema di erogare test, distribuendo il carico tra sito periferico e laboratorio centrale. L’automazione e la standardizzazione dei workflow riducono passaggi manuali e consentono di spostare una parte dell’attività verso i siti periferici, lasciando al laboratorio centrale le analisi a maggiore complessità.[4]
Dal punto di vista organizzativo, decentralizzare permette anche di affrontare meglio la carenza cronica di personale di laboratorio. Invece di concentrare tutta la domanda in un unico nodo, il sistema può distribuire una parte del carico su reparti e territori, mantenendo al centro governance, qualità e conferme specialistiche. Questo non sostituisce il laboratorio centrale, ma lo usa in modo più efficiente.
6. Modelli regionali e ibridi: dall’hub & spoke al network diffuso
La diagnostica decentralizzata può essere implementata con diversi modelli organizzativi. Non esiste un unico approccio valido per tutti; spesso la soluzione ottimale è un modello ibrido, che combina punti di test periferici con un laboratorio centrale di riferimento.
Un modello comune è l’hub & spoke: un laboratorio centrale (hub) supervisiona e supporta punti periferici (spoke) che eseguono i test più urgenti. In una rete diagnostica nazionale o regionale, questo schema può ampliare la copertura territoriale riducendo investimenti infrastrutturali e dispersione di competenze.[12]
Un altro modello è la distribuzione totale, in cui ogni punto di cura dispone di capacità diagnostica molecolare. Questo approccio è utile in contesti molto distribuiti o in situazioni di emergenza, ma richiede maggiore coordinamento, governance dei dati e standardizzazione dei processi.[12]
Confronto tra modello diagnostico tradizionale vs modello distribuito
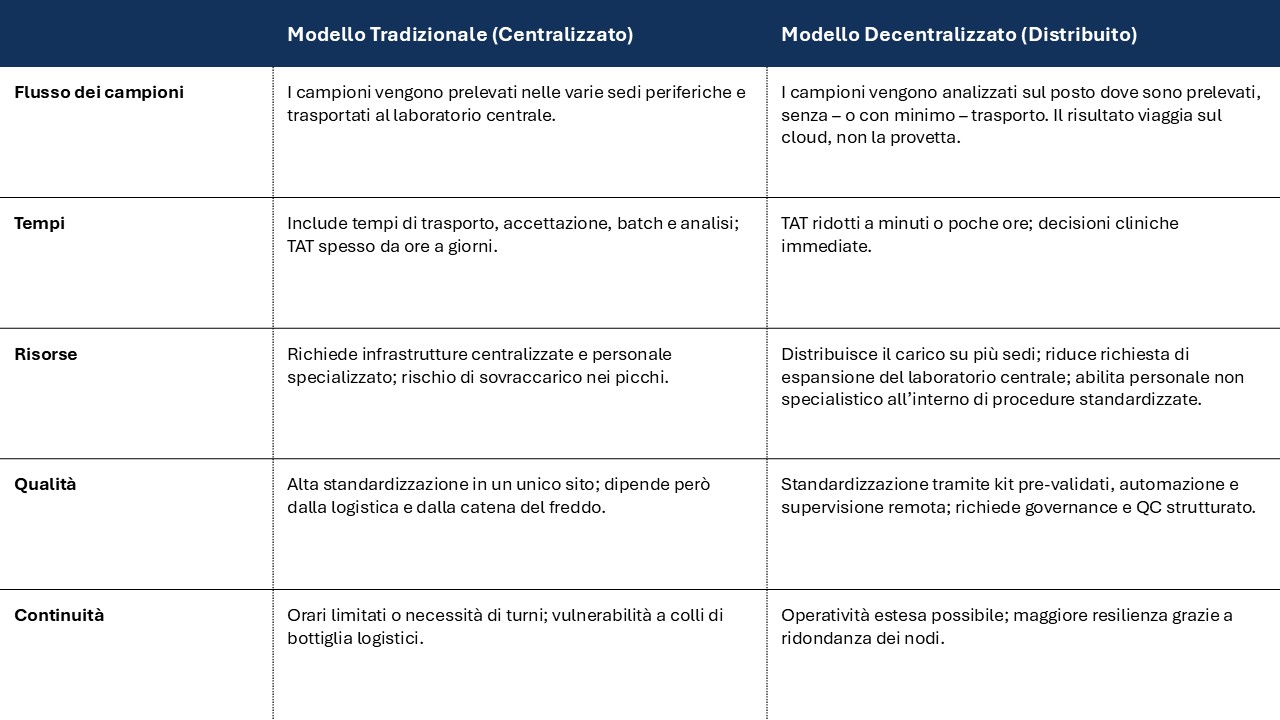
(Il modello ibrido Hub & Spoke combina elementi di entrambi: trasporto ridotto ma non eliminato, test POC su urgenze e hub per conferme o alta produzione, personale locale che esegue il primo screening e hub centrale che mantiene standard e gestisce i casi complessi.)
7. Conclusioni
La diagnostica molecolare decentralizzata rappresenta oggi una delle innovazioni più promettenti per coniugare efficacia clinica ed efficienza operativa. Attraverso reagenti stabilizzati, dispositivi PCR portatili e software di gestione, la diagnostica molecolare avanzata può essere portata più vicino al punto di cura.[1] In sistemi validati questo approccio si è associato a tempi di risposta più rapidi e a un migliore allineamento tra diagnosi e decisione clinica.[13]
I dati mostrano che non si tratta solo di velocizzare il test, ma di tradurre la rapidità in outcome migliori: meno attese inutili, maggiore appropriatezza terapeutica e interventi più tempestivi. Nel COV-19POC, ad esempio, il passaggio da un TAT medio di 21,3 ore a 1,7 ore ha avuto un impatto diretto sull’allocazione dei pazienti e sulla gestione dell’isolamento.[5]
Dal lato operativo e gestionale, la decentralizzazione alleggerisce il peso sui grandi laboratori e rende più reattive le strutture periferiche. Questa distribuzione della capacità diagnostica aumenta la resilienza del sistema, soprattutto quando la domanda cresce rapidamente o quando il contesto logistico rende difficile il ricorso esclusivo al laboratorio centrale.[3]
Naturalmente, ogni innovazione comporta sfide: implementare una diagnostica decentralizzata richiede investimenti iniziali, formazione capillare, integrazione informatica e un cambio di mentalità. Bisogna stabilire governance chiara, garantire controlli di qualità e assicurare che i dati prodotti siano affidabili e integrati nei sistemi informativi. Tuttavia, la letteratura disponibile mostra che le barriere organizzative possono essere affrontate con modelli adeguati di standardizzazione, supervisione e rete.[4]
Dal punto di vista strategico, adottare soluzioni di diagnostica decentralizzata è diventato un elemento di competitività e sostenibilità per molte organizzazioni sanitarie. Un ospedale che riduce i tempi di diagnosi e ottimizza il percorso clinico migliora la qualità della cura; un sistema sanitario regionale che distribuisce capacità diagnostica diventa più resiliente e più equo nell’accesso alle cure.
Con “Diagnostica decentralizzata: efficienza operativa e clinica” abbiamo voluto fornire uno sguardo completo – dati, esempi, modelli organizzativi – su come questa evoluzione impatti positivamente sia la gestione sanitaria sia la vita dei pazienti. La decentralizzazione molecolare non è solo una tecnologia: è un cambio di paradigma che accelera la medicina e ridisegna l’organizzazione dei servizi diagnostici.
In futuro, possiamo attenderci ulteriori progressi: l’integrazione di intelligenza artificiale più sofisticata per predire focolai o supportare l’interpretazione dei risultati, l’ampliamento dei menu di test multiplex e la diffusione di modelli di rete diagnostica sempre più capillari. In conclusione, decentralizzare la diagnostica significa accelerare la medicina. Efficienza operativa e clinica possono finalmente procedere insieme.
Fonti e Bibliografia
[1] Nagaraj S, Ramlal S, Kingston JJ, et al. Thermostabilization of indigenous multiplex polymerase chain reaction reagents for detection of enterotoxigenic Staphylococcus aureus. J Microbiol Immunol Infect. 2018;51(2):191-198. DOI: 10.1016/j.jmii.2016.04.004. PubMed: https://pubmed.ncbi.nlm.nih.gov/27260780/
[2] Martinelli F, Ciccozzi M, Al Moghazi S, et al. Application of a portable instrument for rapid and reliable detection of SARS-CoV-2 infection in any environment. Immunol Rev. 2020;295 Suppl 1:4-10. DOI: 10.1111/imr.12857. PubMed: https://pubmed.ncbi.nlm.nih.gov/32329102/
[3] ECDC. Assessment of point-of-care testing devices for infectious disease surveillance, prevention and control – a mapping exercise. 2022. https://www.ecdc.europa.eu/en/publications-data/assessment-point-care-testing-devices-infectious-disease-surveillance-prevention
[4] Drancourt M, Michel-Lepage A, Boyer S, Raoult D. The point-of-care laboratory in clinical microbiology. Clin Microbiol Rev. 2016;29(3):429-447. DOI: 10.1128/CMR.00090-15. PubMed: https://pubmed.ncbi.nlm.nih.gov/27029593/
[5] Brendish NJ, Poole S, Naidu VV, et al. Clinical impact of molecular point-of-care testing for suspected COVID-19 in hospital (COV-19POC): a prospective, interventional, non-randomised, controlled study. Lancet Respir Med. 2020;8(12):1192-1200. DOI: 10.1016/S2213-2600(20)30454-9. PubMed: https://pubmed.ncbi.nlm.nih.gov/33038974/
[6] Mojebi A, Wu P, Keeping S, et al. Clinical impact of rapid molecular diagnostic tests in patients presenting with viral respiratory symptoms: a systematic literature review. PLoS One. 2024;19(6):e0303560. DOI: 10.1371/journal.pone.0303560. PubMed: https://pubmed.ncbi.nlm.nih.gov/38870136/
[7] Tan C, Chan CK, Ofner M, et al. Implementation of point-of-care molecular testing for respiratory viruses in congregate living settings. Infect Control Hosp Epidemiol. 2024;45(9):1085-1089. DOI: 10.1017/ice.2024.72. PubMed: https://pubmed.ncbi.nlm.nih.gov/38659123/
[8] Boeke CE, Joseph J, Wang M, et al. Point-of-care testing can achieve same-day diagnosis for infants and rapid ART initiation: results from government programmes across six African countries. J Int AIDS Soc. 2021;24(3):e25677. DOI: 10.1002/jia2.25677. PubMed: https://pubmed.ncbi.nlm.nih.gov/33745234/
[9] Bissonnette L, Bergeron MG. Portable devices and mobile instruments for infectious diseases point-of-care testing. Expert Rev Mol Diagn. 2017;17(5):471-494. DOI: 10.1080/14737159.2017.1310619. PubMed: https://pubmed.ncbi.nlm.nih.gov/28343420/
[10] Simmonds FM, Cohn J, Moyo C, et al. Task shifting for point-of-care early infant diagnosis: a comparison of the quality of testing between nurses and laboratory personnel in Zimbabwe. Hum Resour Health. 2020;18(1):4. DOI: 10.1186/s12960-020-0449-2. PubMed: https://pubmed.ncbi.nlm.nih.gov/31992332/
[11] le Roux SM, Dramowski A, Finlayson H, et al. Cost-effectiveness of point-of-care versus centralised, laboratory-based nucleic acid testing for diagnosis of HIV in infants: a systematic review of modelling studies. Lancet HIV. 2023;10(5):e320-e331. DOI: 10.1016/S2352-3018(23)00029-2. PubMed: https://pubmed.ncbi.nlm.nih.gov/37149292/
[12] Mataka A, Tumbare EAJ, Holtzman D, et al. Strategic site selection for placement of HIV early infant diagnosis point-of-care technology within a national diagnostic network in Lesotho. Afr J Lab Med. 2021;10(1):1156. DOI: 10.4102/ajlm.v10i1.1156. PubMed: https://pubmed.ncbi.nlm.nih.gov/34522629/
[13] Miscio L, Olivieri A, Labonia F, et al. Evaluation of the diagnostic accuracy of a new point-of-care rapid test for SARS-CoV-2 virus detection. J Transl Med. 2020;18(1):488. DOI: 10.1186/s12967-020-02651-y. PubMed: https://pubmed.ncbi.nlm.nih.gov/33349261/
[14] Padoan A, Cosma C, Aita A, et al. Hyris bCUBE SARS-CoV-2 rapid molecular saliva testing: a POCT innovation on its way. Clin Chem Lab Med. 2022;60(5):766-770. DOI: 10.1515/cclm-2022-0008. PubMed: https://pubmed.ncbi.nlm.nih.gov/35041302/
[15] Hansen GT. Point-of-Care Testing in Microbiology: A Mechanism for Improving Patient Outcomes. Clin Chem. 2020;66(1):124-137. DOI: 10.1373/clinchem.2019.304782. PubMed: https://pubmed.ncbi.nlm.nih.gov/31811002/